Anilin
V dnešním světě se Anilin stalo tématem velkého významu a zájmu velkého množství lidí. Ať už kvůli svému dopadu na společnost, historickému významu nebo vlivu na různé aspekty každodenního života, Anilin upoutal pozornost širokého publika. Od svých počátků až po současnou evoluci Anilin nadále vytváří debaty, úvahy a hluboké analýzy. V tomto článku prozkoumáme různé aspekty související s Anilin s cílem ponořit se do jeho důležitosti a lépe porozumět jeho dopadu na moderní svět.
| Anilin | |
|---|---|
 Strukturní vzorec anilinu | |
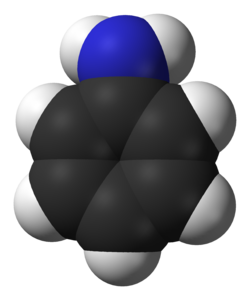 Prostorový model | |
| Obecné | |
| Systematický název | fenylamin |
| Triviální název | anilin |
| Funkční vzorec | C6H5NH2 |
| Sumární vzorec | C6H7N |
| Vzhled | bezbarvá (na světle žloutnoucí) kapalina s charakteristickým zápachem |
| Identifikace | |
| Registrační číslo CAS | 62-53-3 |
| EC-no (EINECS/ELINCS/NLP) | 200-539-3 |
| Indexové číslo | 612-008-00-7 |
| Vlastnosti | |
| Molární hmotnost | 93,13 g/mol |
| Teplota tání | −6,3 °C |
| Teplota varu | 184,13 °C |
| Hustota | 1,027 g/cm³ |
| Viskozita | 4,4 mPa•s (20 °C) |
| Disociační konstanta pKb | 9,37 |
| Rozpustnost ve vodě | 36 g/l (20 °C) |
| Struktura | |
| Dipólový moment | 1,55 D |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H351 H341 H331 H311 H301 H372 H318 H317 H400 |
| R-věty | R23/24/25 R40 R41 R43 R48/23/24/25 R68 R50 |
| S-věty | S1/2 S26 S27 S36/37/39 S45 S46 S61 S63 |
Některá data mohou pocházet z datové položky. | |
Anilin, systematicky fenylamin, je bezbarvá olejovitá kapalina. Na vzduchu snadno oxiduje a barví se na žlutou až hnědou barvu. Je toxický, má zásaditou reakci. Také je to v největším množství vyráběná organická zásada.
Používaný název aminobenzen není systematický (lze ho pokládat za polotriviální), neboť přítomnost aminové skupiny se v uhlovodíkovém řetězci vyjadřuje primárně příponou -amin.[2]
V přírodě se anilin nachází v černouhelném dehtu, průmyslově se vyrábí redukcí nitrobenzenu. Používá se při výrobě barviv, léčiv, plastů a gumárenských chemikálií (pomáhá urychlovat přeměnu kaučuku na pryž, tzv. vulkanizaci).[3] V současnosti má tato látka největší využití jako reakční komponenta při výrobě polyuretanů.
Příprava
Průmyslově se anilin vyrábí většinou z benzenu, a to ve dvou krocích. Prvním krokem je nitrace benzenu pomocí nitrační směsi kyseliny dusičné a kyseliny sírové. Vzniklý nitrobenzen se poté hydrogenuje při teplotě 600 °C za použití katalyzátoru niklu.
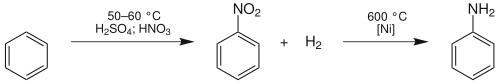
Další používanou technologií je proces vyvinutý v České republice prof. Paškem z VŠCHT Praha. Jeho podstatou je hydrogenace nitrobenzenu na anilin na měděném katalyzátoru při teplotě 215 °C. Tímto procesem se v současnosti vyrábí asi 10 % světové výroby anilinu[zdroj?] a je realizován v BCH MCHZ Ostrava a licenčně v Japonsku. Další jednotky jsou projektovány mj. v Rusku.[zdroj?]
V laboratoři se používá redukce nitrobenzenu v prostředí kyseliny chlorovodíkové s železem.
Toxicita
K otravě dochází požitím, nadýcháním nebo vstřebáním kůži. Projevuje se cyanózou (modrofialové zbarvení kůže a sliznic způsobené nedostatečným okysličováním krve). Anilin je krevní jed a způsobuje oxidaci krevního barviva hemoglobinu na methemoglobin. Působí také na centrální nervový systém, proto postižený jeví podobné známky jako opilec. Zmodrání kůže se projevuje v první řadě na rtech, uších, nosu a nehtech. Dalším symptomem je bolest hlavy. Smrtelná dávka je 1 g, snižuje se však účinkem ethanolu.[zdroj?]
Po požití jako první pomoc podáme 100–200 ml parafinového oleje (ne však jiného oleje či tuku!) a vyvoláme zvracení. Doporučená je konzumace černé kávy.[zdroj?] Nesmí se podávat mléko, alkohol či tuky. Postiženého uložíme na čerstvý vzduch a zařídíme převoz k nemocničnímu ošetření.
Chemické reakce
Aromatická elektrofilní substituce
Dusík v aminové skupině má volný elektronový pár, který jednak způsobuje zásadité vlastnosti (dle Lewisovy teorie kyselin a zásad) a jednak aktivuje benzenové jádro pro elektrofilní substituce. Substituční reakce dokonce probíhá tak rychle, že je obtížné ji zastavit v prvním kroku[zdroj?] a vznikají trisubstituované deriváty. Obsazují polohy ortho a para vzhledem k aminoskupině. Možností, jak připravit monosubstituovaný derivát, je oslabit účinek aminoskupiny acetylací za vzniku acetanilidu a v dalším kroku provést substituci.
Diazotace a kopulace
Diazotace a kopulace jsou základní reakce pro přípravu barevných látek, jako například Sudan III, který má ohnivě červenou barvu. Tato barviva se obecně nazývají azosloučeniny, protože obsahují azo skupinu : -N=N-.
- Nejprve se reakcí anilinu s dusitanem v prostředí zředěné kyseliny chlorovodíkové připraví benzendiazoniová sůl. To je poměrně stálá pevná látka iontového charakteru. Na obou dusících je delokalizovaný kladný náboj a chlor je zde ve formě chloridu.
- V druhém kroku dochází ke kopulaci benzendiazoniové soli s nukleofilním činidlem, které má přebytek elektronů. Vzniká azosloučenina. Pokud je nukleofilním činidlem aromát – například fenol nebo arylamin –, pak je ve výsledné molekule konjugovaný systém dvojných a jednoduchých vazeb, který je zachycuje kvanta světelného záření a látka se jeví jako barevná.
Kontaminace nylonového nádobí
Spolu s dalšími primárními aminy se může uvolňovat z nylonového nádobí. Pravděpodobně proto, že k jeho barvení užívají azobarviva a primární aminy se uvolňují v důsledku působení vysokých teplot při styku nádobí s horkými potravinami.[4]
Reference
- ↑ a b Aniline. pubchem.ncbi.nlm.nih.gov . PubChem . Dostupné online. (anglicky)
- ↑ KOTVALTOVÁ SEZEMSKÁ, KAROLÍNA, 1990-. Názvosloví organických sloučenin. Vydání 2., upravené. vyd. Praha: 239 s. Dostupné online. ISBN 978-80-200-3075-7, ISBN 80-200-3075-1. OCLC 1143810036
- ↑ Otec českých organických technologií | Technický týdeník. www.technickytydenik.cz . . Dostupné online.
- ↑ Co se může uvolňovat z černého plastového nádobí? Okem nic nepoznáte
Literatura
- Svoboda, Jiří: Organická chemie I, Vysoká škola chemicko-technologická, Praha 2005
Externí odkazy
 Obrázky, zvuky či videa k tématu Anilin na Wikimedia Commons
Obrázky, zvuky či videa k tématu Anilin na Wikimedia Commons




