Organické sloučeniny hliníku
V dnešním článku prozkoumáme fascinující svět Organické sloučeniny hliníku, téma, které přitahuje pozornost společnosti již dlouhou dobu. Ať už kvůli svému vlivu na historii, jeho aktuálnosti dnes nebo jeho budoucímu potenciálu, Organické sloučeniny hliníku vyvolal neustálý zájem o různé oblasti a byl předmětem četných debat a studií. V tomto článku se pokusíme analyzovat různé aspekty související s Organické sloučeniny hliníku, od jeho vzniku až po jeho možné důsledky v budoucnosti, s cílem nabídnout komplexní vizi tohoto vzrušujícího tématu.

Organické sloučeniny hliníku, též organohlinité sloučeniny, jsou chemické sloučeniny obsahující vazby mezi atomy uhlíku a hliníku. Jedná se o jednu z nejdůležitějších skupin organokovových sloučenin.[1][2] Příklady sloučenin jsou dimerní trimethylhliník, monomerní triisobutylhliník a sloučenina titanu a hliníku nazývaná Tebbeovo činidlo. Vlastnosti organohlinitých sloučenin lze vysvětlit skrz polaritu vazby C−Al a vysokou Lewisovskou kyselostí trikoordinovaných sloučenin.
V průmyslu se tyto sloučeniny nejčastěji používají na výrobu polyalkenů.
Historie
První organohlinitá sloučenina, (C2H5)3Al2I3, byla objevena v roce 1859.[3] Větší rozvoj nastal v 50. letech 20. století, kdy Karl Ziegler objevil přímou přípravu trialkylhlinitých sloučenin a zapojil je do katalytických polymerizací alkenů. Za tento objev poté získal Nobelovu cenu za chemii.
Struktura
Hlinité sloučeniny
Organohlinité sloučeniny mají obvykle tříkoordinovaná nebo čtyřkoordinovaná Al centra, u anorganických ligandů, jako například fluoridových aniontů, byla zjištěna i vyšší koordinační čísla. Jak je běžné i v jiných případech, tak čtyřkoordinované atomy nejčastěji vytváří tetraedrické struktury. Oproti boru má hliník větší atom a snadněji na sebe naváže čtyři uhlíkové ligandy. Triorganohlinité sloučeniny jsou tak často dimerní s dvojicí můstkových alkylových ligandů, příkladem může být sloučenina Al2(C2H5)4(μ-C2H5)2;i když bývá obvykle nazývána triethylhlíník, tak obsahuje dvě Al centra a šest ethylových skupin. Pokud organohlinitá sloučenina obsahuje hydridovou nebo halogenidovou skupinu, tak obvykle můstky vytváří tyto menší ligandy. Koordinační číslo 3 se objevuje, když jsou na hliník navázány rozměrné skupiny, například mesityl u trimesitylhliníku, Al(Mes)3, či isobutyl.[4]

Výměna ligandů v trialkylahlinitých sloučeninách
Trialkylhlinité sloučeniny často vytvářejí dynamické rovnováhy, vedoucí k výměnám můstkových a koncových ligandů i ligandů mezi dimery. I nekoordinujících rozpouštědlech probíhá výměna Al-Me velmi rychle, to bylo potvrzeno spektroskopií protonové nukleární magnetické rezonance; při −25 °C obsahovalo 1H NMR spektrum Me6Al2 dva signály v poměru 1:2, jak bylo očekáváno na základě struktury pevné formy. Při 20 °C byl pozorován pouze jeden signál, protože byla výměna koncových a můstkových methylových skupin příliš rychlá, než aby mohla být rozlišena pomocí NMR.[5] Vysoká Lewisovská kyselost monomerních částic je dána velikostí hlinitého centra a jeho snahou o dosažení elektronového oktetu.
Organické sloučeniny hliníku v nízkých oxidačních číslech
První organohlinitá sloučenina s vazbami Al-Al byla popsána roku 1988, šlo o (((Me3Si)2CH)2Al)2. Takovéto molekuly se obvykle získávají redukcemi dialkylhlinitých chloridů draslíkem:[6]
- (R2AlCl)2 + 2 K → R2Al-AlR2 + 2 KCl
Další významnou skupinou jsou tetraalany obsahující čtyři Al+ centra. Mají tetraedranová jádra, jak lze vidět na následujícím znázornění (Cp*Al)4 a ((Me3Si3C)Al)4. Shluk 2− byl vytvořen při výzkumu redukce organohlinitých sloučenin. Tento dianion má strukturu dvacetistěnu odpovídající dodekaboritanovému aniontu (2−). Formální oxidační číslo hliníku je zde menší než 1..
Příprava a výroba
Z alkylhalogenidů a hliníku
Průmyslově se jednoduché alkylované sloučeniny hliníku typu Al2R6 (R = Me, Et) vyrábějí v dvoufázovém procesu, který začíná alkylací práškového hliníku:
- 2 Al + 3 CH3CH2Cl → (CH3CH2)3Al2Cl3
Reakce je podobná výrobě Grignardových činidel. Produkt se vzorcem (CH3CH2)3Al2Cl3lze následně převést na triorganohlinité sloučeniny pomocí redukce:
- 2 (CH3CH2)3Al2Cl3 + 6 Na → (CH3CH2)6Al2 + 2 Al + 6 NaCl
Tento postup se používá na výrobu trimethylhliníku a triethylhliníku.[7]
Hydroalumince
Práškový hliník za přítomnosti vodíku přímo reaguje s některými koncovými alkeny. Proces se skládá ze dvou částí, v první se vytvoří dialkylhlinité hydridy. Reakce se obvykle provádí za vyšších teplot a vyžadují aktivaci trialkylhlinitými sloučeninami:
- 6 Al + 3 H2 + 12 CH2=CHR → 2 3
Pokud R skupina není příliš objemná, tak bývá produkt většinou trimerní. V následujícím kroku reaguje hydrid s dalším přídavkem alkenu a vznikne konečný produkt:
- 2 3 + 3 CH2=CHR → 3 [Al2(CH2CHR)3
Diisobutylhliník, jenž vytváří dimer, se získává hydridovou eliminací z triisobutylhliníku:
- 2 i-Bu3Al → (i-Bu2AlH)2 + 2 (CH3)2C=CH2
Karboaluminace
Organohlinité sloučeniny mohou reagovat s alkeny a alkyny za adice jedné organylové skupiny a kovu na násobnou vazbu; tato reakce se nazývá karboaluminace; může probíhat čistě tepelně za katalýzy přechodným kovem. Při nekatalyzované reakci je u substituovaných alkenů možná pouze monoadice. Při použití ethenu mají vzniklé produkty Poissonovo rozdělení vyšších alkylaluminovaných sloučenin. Reakce je u 1-alkenů regioselektivní.[8] ZACA reakce, kterou objevil Eiči Negiši, je asymetrická karboaluminace alkenů katalyzovaná derivátem zirkonocenu.[9]
Methylaluminace alkynů za přítomnosti Cp2ZrCl2[10][11] se používá na stereospecifickou přípravu trisubstituovaných alkenů, které jsou často obsaženy v terpenech a polyketidech. Syntézu (E)-4-jodo-3-methylbut-3-en-1-olu[12], znázorněnou níže, je jednou z těchto reakcí:
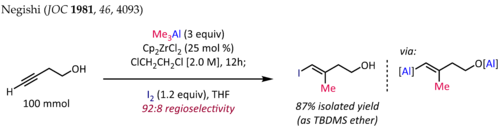
U koncových alkynů mívá reakce dobrou regioselektivitu (>90:10) a je výhradně syn-selektivní, a to i tehdy, když se v reakční směsi nachází propargylové či homopropargylové substituenty na heteroatomu. Při rozšiřování toho postupu na alkylaluminace vyššími alkyly byly ovšem dosaženy nižší výtěžnosti a špatné regioselektivity.
Příprava v laboratoři
I když jsou nižší alkylhlinité sloučeniny komerčně dostupné a nepříliš drahé, tak byla vyvinuta řada způsobů jejich laboratorní přípravy, například pomocí podvojných záměn nebo transmetalace. Reakcemi chloridu hlinitého s RLi nebo RMgX vznikají trialkylované sloučeniny:
- AlCl3 + 3 BuLi → Bu3Al + 3 LiCl
Transmetalace:
- 2 Al + 3 HgPh2 → 2 AlPh3 + 3 Hg
Reakce
V důsledku rozdělení nábojů mezi atomy hliníku a uhlíku organohlinité sloučeniny snadno reagují s elektrofily.
Lewisovská kyselost
Organohlinité sloučeniny patří podle teorie HSAB mezi tvrdé kyseliny a tvoří adukty se zásadami, například pyridinem, tetrahydrofuranem a terciárními aminy. Tyto adukty mají tetraedrické Al centra.
Reakce s elektrofily
Vazba Al–C je polarizovaná a atom uhlíku navázaný na hliník je tak silně zásaditý. Reakcemi organohlinitých sloučenin s kyselinami vznikají alkany, s alkoholy se vytváří alkoxidy:
- AlR'3 + ROH → 1/n (R'2Al−OR)n + R'H
Lze použít mnoho různých kyselin, i jednoduché minerální kyseliny.
Reakcemi s aminy vznikají amidové deriváty. Reakcemi oxidu uhličitého s trialkylhlinitými sloučeninami se vytváří dialkylhlinité karboxyláty a následně alkylhlinité dikarboxyláty:
- AlR3 + CO2 → R2AlO2CR
- R2AlO2CR + CO2 → RAl(O2CR)2
Přeměna se podobá karbonaci Grignardových činidel.[13][14][15]
Podobně se reakcemi trialkylhlinitých sloučenin s oxidem uhličitým dají připravit alkoholy, alkeny[13] nebo ketony.[16]
Působením kyslíku lze získat příslušné alkoxidy, jež mohou být hydrolyzovány na alkoholy:
- AlR3 + 3/2 O2 → Al(OR)3
Je znám také organohlinitý organický peroxid 2}Al(R)-O-O-CMe3] .[17]
Reakce čistých trialkylhlinitých sloučenin s vodou, alkoholy, fenoly, aminy, oxidem uhličitým, oxidy síry, oxidy dusíku, halogeny a halogenovanými uhlovodíky mohou být nebezpečné.[18][19]
Polymerizace alkenů
V průmyslu se organohlinité sloučeniny, jako je methylaluminoxan, používají jako katalyzátory polymerizace alkenů.
Reference
V tomto článku byl použit překlad textu z článku Organoaluminium chemistry na anglické Wikipedii.
- ↑ D. F. Shriver; P. W. ATKINS. Inorganic Chemistry. : Oxford University Press, 2006. ISBN 978-0199264636.
- ↑ M. Witt; H. W. ROESKY. Organoaluminum chemistry at the forefront of research and development. Current Science. 2000, s. 410. Dostupné v archivu pořízeném dne 2014-10-06.
- ↑ Hallwachs, W.; SCHAFARIK, A. Ueber die Verbindungen der Erdmetalle mit organischen Radicalen. Liebigs Annalen. 1859, s. 206–209. Dostupné online. doi:10.1002/jlac.18591090214.
- ↑ C. Elschenbroich. Organometallics. 3rd. vyd. Weinheim: Wiley-VCH, 2006. ISBN 978-3-527-29390-2.
- ↑ COTTON, Frank Albert; WILKINSON, GEOFFREY. Advanced Inorganic Chemistry. : , 1980. ISBN 978-0-471-02775-1. S. 343.
- ↑ Uhl, W. Organoelement Compounds Possessing Al-Al, Ga-Ga, In-In, and Tl-Tl Single Bonds. : , 2004. ISBN 9780120311514. doi:10.1016/S0065-3055(03)51002-4. S. 53–108.
- ↑ Michael J. Krause, Frank Orlandi, Alfred T. Saurage and Joseph R. Zietz "Aluminum Compounds, Organic" in Ullmann's Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim doi:10.1002/14356007.a01_543
- ↑ Barry M. Trost; MARTIN F. SEMMELHACK; IAN FLEMING. Comprehensive Organic Synthesis: Additions to and substitutions at C-C-Bonds. : Pergamon, 1992. ISBN 9780080405957.
- ↑ NEGISHI, Ei-ichi. Discovery of ZACA reaction : Zr-catalyzed asymmetric carboalumination of alkenes. Arkivoc. 2011, s. 34–53. Dostupné online. doi:10.3998/ark.5550190.0012.803.
- ↑ NEGISHI, Ei-ichi; WANG, Guangwei; RAO, Honghua; XU, Zhaoqing. Alkyne Elementometalation−Pd-Catalyzed Cross-Coupling. Toward Synthesis of All Conceivable Types of Acyclic Alkenes in High Yields, Efficiently, Selectively, Economically, and Safely: "Green" Way. The Journal of Organic Chemistry. 2010-05-14, s. 3151–3182. doi:10.1021/jo1003218. PMID 20465291.
- ↑ NEGISHI, Ei-ichi. Organometallics In Synthesis: A Manual (Ed. M. Schlosser). Chichester, West Sussex, UK: Wiley, 2002. ISBN 978-0471984160. S. 963–975.
- ↑ RAND, Cynthia L.; HORN, David E. Van; MOORE, Mark W.; NEGISHI, Eiichi. A versatile and selective route to difunctional trisubstituted (E)-alkene synthons via zirconium-catalyzed carboalumination of alkynes. The Journal of Organic Chemistry. 2002-05-01, s. 4093–4096. doi:10.1021/jo00333a041.
- ↑ a b YUR'EV, V. P.; KUCHIN, A. V.; TOLSTIKOV, G. A. Reaction of aluminum trialkyls with carbon dioxide. Organic and Biological Chemistry. 1974, s. 817–819. doi:10.1007/BF00923507.
- ↑ ZIEGLER, K. Neue Entwicklungen der metallorganischen Synthese. Angew. Chem.. 1956, s. 721–729. doi:10.1002/ange.19560682302.
- ↑ ZAKHARKIN, L. I.; GAVRILENKO, V. V.; IVANOV, L. L. Zh. Obshch. Khim.. 1967, s. 992.
- ↑ David W. Marshall, US patent US3168570, assigned to Continental Oil
- ↑ W. Uhl; B. JANA. A persistent alkylaluminum peroxide: Surprising stability of a molecule with strong reducing and oxidizing functions in close proximity. Chemistry—A European Journal. 2008, s. 3067–3071. doi:10.1002/chem.200701916. PMID 18283706.
- ↑ Cameo Chemicals SDS
- ↑ Handling Chemicals Safely 1980. p. 929
Externí odkazy
 Obrázky, zvuky či videa k tématu Organické sloučeniny hliníku na Wikimedia Commons
Obrázky, zvuky či videa k tématu Organické sloučeniny hliníku na Wikimedia Commons